一、酸堿滴定法
酸堿滴定法是以酸、堿之間質子傳遞反應為基礎的一種滴定分析法。可用于測定酸、堿和兩性物質。其基本反應為H OH- = H2O;
也稱中和法,是一種利用酸堿反應進行容量分析的方法。用酸作滴定劑可以測定堿,用堿作滴定劑可以測定酸,這是一種用途極為廣泛的分析方法。
酸堿滴定法的實際應用:混合堿的測定(雙指示劑法)
NaOH ,Na2CO3 ,NaHCO3, 判斷由哪兩種組成(定性/定量計算);Na2CO3能否直接滴定,有幾個滴定突躍點以HCl為标準溶液,首先使用酚酞作指示劑,變色時,消耗HCl溶液體積V1,再加入甲基橙指示劑, 繼續滴定至變色,又消耗 HCl 溶液體積V2, 如圖所示:
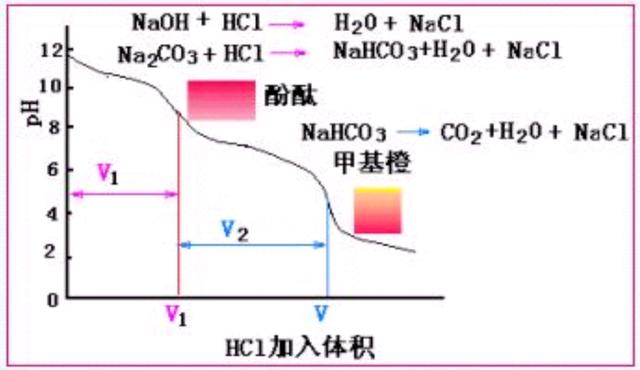
實驗結果與讨論:
(1) 當 V1>V2 時,混合堿組成:NaOH(V1-V2) , Na2CO3(V2)
(2) 當 V1 = V2 時,混合堿組成:Na2CO3
(3) 當 V1<V2 時,混合堿組成:Na2CO3 (V1),NaHCO3 (V2-V1)
(4) 當 V1 =0 時,混合堿組成:NaHCO3
(5) 當 V2 =0 時,混合堿組成:NaOH
二、絡合滴定法
絡合滴定法是以絡合反應(形成配合物)反應為基礎的滴定分析方法,又稱配位滴定。
絡合反應廣泛地應用于分析化學的各種分離與測定中,如許多顯色劑,萃取劑,沉澱劑,掩蔽劑等都是絡合劑。
絡合滴定法的實際應用:
鹽水中Ca2 、Mg2 含量分析:
(1)鈣離子測定
在pH為12~13的堿性溶液中,以鈣—羧酸為指示劑,用EDTA标準溶液滴定樣品,鈣—羧酸為指示劑與鈣離子形成穩定性較差的紅色絡合物,當用EDTA溶液滴定時,EDTA即奪取絡合物中的鈣離子。遊離出鈣—羧酸為指示劑的陰離子,溶液由紅色變為藍色終點,以下用Na2H2Y代表EDTA其反應式如下:
Ca2 NaH2T → CaT- 2H Na
CaT- Na2H2Y → CaY2- 2Na H HT2-
(2)鎂離子測定
用緩沖液調節試樣的pH值約等到于10,以鉻黑T為指示劑用EDTA标準溶液滴定樣品,溶液由紫紅色變為藍色終點。測得鈣鎂離子總量,再從總量中減去鈣離子含量即得鎂離子含量.其反應式如下:
Mg2 2NaH2T → MgT- Na 2H
Na2H2Y MgT - → M gY2- 2Na H HT2-
Ca2 NaH2T → CaT- 2H Na
CaT- Na2H2Y→ CaY2- 2Na H HT2-
EDTA與許多金屬離子形成穩定程度不同的可溶性絡合物,在不同溶液與不同的pH值時,應用不同的掩蔽劑進行直接或間接滴定,故此法叫絡合滴定。
利用掩蔽法對共存離子進行分别測定 :
(1)配位掩蔽法
通過加入一種能與幹擾離子生成更穩定配合物的試劑。
例:測定鈣、鎂離子時,鐵、鋁離子産生幹擾,可采用加入三乙醇胺(能與鐵、鋁離子生成更穩定的配合物)來掩蔽幹擾離子鐵、鋁離子。
(2)氧化還原掩蔽法
例如:Fe3 幹擾Zr2 的測定,加入鹽酸羟胺等還原劑使Fe3 還原生成Fe2 ,達到消除幹擾的目的。
(3)沉澱掩蔽法
例如:為消除Mg2 對Ca2 測定的幹擾,利用pH≥12時,Mg2 與OH-生成Mg(OH)2沉澱,可消除Mg2 對Ca2 測定的幹擾。
三、氧化還原滴定法
氧化還原滴定法是以氧化還原反應為基礎的容量分析方法。
它以氧化劑或還原劑為滴定劑,直接滴定一些具有還原性或氧化性的物質;或者間接滴定一些本身并沒有氧化還原性,但能與某些氧化劑或還原劑起反應的物質。
氧化還原滴定法的實際應用:高考考查頻率很高的是碘量法。
碘量法的特點:碘量法是基于I2氧化性及I-的還原性所建立的氧化還原分析法。

I2是較弱的氧化劑,I-是中等強度的還原劑,用I2标準溶液直接滴定還原劑的方法是直接碘量法;利用I-與強氧化劑作用生成定量的I2,再用還原劑标準溶液與I2反應,測定氧化劑的方法稱為間接碘法,也稱碘量法。
碘量法的基本反應是:
I2 2S2O32- = S4O62- 2I-
該反應在中性或弱酸性中進行,pH過高,I2會發生歧化反應,在強酸性溶液中,Na2S2O3會發生分解,I-容易被氧化。通常pH<9。
四、沉澱滴定法
沉澱滴定法是利用沉澱反應進行容量分析的方法。生成沉澱的反應很多,但符合容量分析條件的卻很少,沉澱滴定實際上應用最多的是銀量法。
沉澱滴定法的實際應用:
鹽水中的氯化鈉含量測定:
在中性溶液中,硝酸銀與氯化鈉反應生成白色的氯化銀沉澱,當氯化鈉反應完畢後,硝酸銀立即與鉻酸鉀作用,生成磚紅色的鉻酸銀沉澱。其反應式如下:
NaCl AgNO3 → AgCl↓(白色) NaNO3
2AgNO3 K2CrO4→ Ag2CrO4 ↓(磚紅色) 2KNO3
本法必須控制在中性或微堿性溶液(pH值6.5—10.5)中滴定,在酸性溶液中,由于鉻酸銀溶于酸,使滴定結果偏高,而在堿性溶液中,銀離子又生成灰黑色氧化銀沉澱,影響滴定和終點的判定。
在滴定過程中,生成的氯化銀沉澱能吸附氯離子,鉻酸銀沉澱将過早地出現,因此滴定時必須劇烈震蕩溶液,使吸附的氯離子重新反應生成氯化銀沉澱。
佛爾哈德(Volhard)法:直接滴定法(測Ag )
在酸性介質中,鐵铵礬作指示劑,用NH4SCN标準溶液滴定Ag ,當AgSCN 沉澱完全後,過量的 SCN- 與 Fe3 反應:
Ag SCN- = AgSCN↓(白色)
Fe3 SCN- = FeSCN2 (紅色絡合物)
五、四大滴定法的異同點
共同點:
1、他們都是以消耗計算量的标準物質來測定被測物質含量的。
2、随着滴定劑的加入,被滴定物質的濃度在計量點附近會有突變(突躍),可以用這一突變,或通過這一突變導緻指示劑的變色來制定滴定終點。
3、滴定分析終點誤差的定義都可以表示為Et={【(cV)T-(cV)X】/(cV)X}*100%。
4、由于曆史遺留問題四者使用的常數不同,若都用滴定常數Kt,可使四種滴定數學處理趨于一緻。
不同點:
1、強酸強堿的滴定産物為水,從滴定未開始到滴定結束【H20】一直是一個常數,約為55.5mol/L。
2、沉澱滴定有異相生成随着滴定的進行,一旦有沉澱生成他的活度就被制定為1,并且保持不變。
3、絡合滴定産物ML的濃度在滴定過程中是一變量開始時為0,随着滴定的進行,ML的濃度近線性的增大,直至化學計量點。
4、最簡單的氧化還原反映的滴定産物有兩種,他們在滴定過程中的濃度變化與絡合滴定産物ML相似。所以從這一意義上,可把滴定分析分為兩種,一種是滴定産物的濃度為常量的,如強酸強堿滴定、沉澱滴定;一種是産物為變量的,如絡合和氧化還原滴定。
六、四大滴定法的指示劑指示劑比較
指示劑在分析滴定中是一支神奇的“魔棒”他指示着我們實驗的進程,以便使我們知道什麼時候開始以及什麼時候結束。
酸堿指示劑:一些有機弱酸或弱堿,它們的酸式或堿式具有不同的顔色。
金屬指示劑:與酸堿指示劑不同,它不是以指示溶液中H 的濃度變化确定終點,而是以指示溶液中金屬離子的濃度變化确定終點。
氧化還原指示劑:一些有機物随氧化還原電位變化而改變顔色,從而達到指示終點的目的。
吸附指示劑:它是沉澱指示劑中的一類特殊指示劑。
指示劑的适用條件:
1、每種酸堿指示劑都有一定的變色範圍。
2、金屬指示劑絡合物與指示劑的顔色有明顯區别,終點顔色變化才明顯。金屬指示劑絡合物穩定性應比金屬-EDTA絡合物的穩定性要低。
3、氧化還原指示劑是一種通用的指示劑,應用比較廣泛。
4、盡量使沉澱表面積大些
,